原标题:我国首个单剂新冠疫苗来了!国内四款疫苗有啥不同?
2月25日晚,国家药监局附条件同意国药集团新冠灭活疫苗(Vero细胞)和康希诺重组新冠疫苗(5型腺病毒载体)注册请求。其间,康希诺的新冠疫苗是首款获批的国产腺病毒载体新冠病毒疫苗,也是仅有选用单针免疫程序的新冠疫苗。
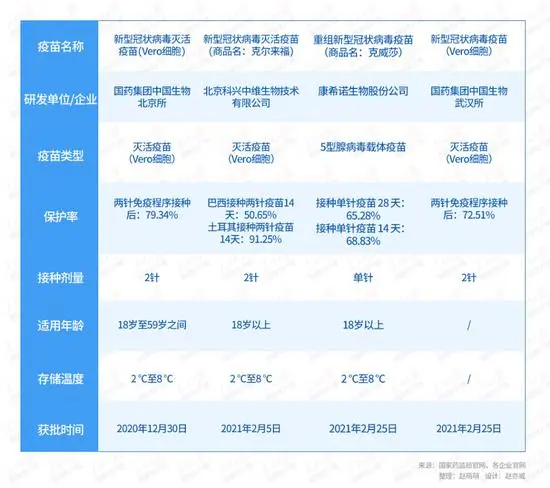
至此,国内已有4款新冠疫苗获批上市,其间包含3款新冠灭活疫苗和1款腺病毒载体疫苗。
国药中生武汉所新冠疫苗,4天火速获批
2月21日,国药集团我国生物武汉所向国家药监局提交新冠病毒灭活疫苗(Vero细胞)附条件上市请求,从递送上市请求到正式获批仅用时4天。研讨所2月24日发布的新冠灭活疫苗Ⅲ期临床试验期中剖析数据显现,该疫苗接种后安全性杰出,两针免疫程序接种后,疫苗接种者均发生高滴度抗体,中和抗体阳转率为99.06%,疫苗针对由新冠病毒感染引起的疾病(COVID-19)的维护效能为72.51%。
重组新式冠状病毒疫苗。图片来源于康希诺官网。
康希诺克威莎,首款国产单剂腺病毒载体新冠病毒疫苗
康希诺生物与陈薇院士团队一起研制重组新冠病毒疫苗(5型腺病毒载体)(Ad5-nCoV)克威莎是首款获批的国产腺病毒载体新冠病毒疫苗,也是仅有选用单针免疫程序的新冠疫苗,可于2°C至8°C之间安稳保存。
克威莎的Ⅲ期临床试验期中剖析数据成果显现,单针接种疫苗28天后,疫苗对一切症状的整体维护效能为65.28%;在单针接种疫苗14天后,疫苗对一切症状整体维护效能为68.83%。疫苗对重症的维护效能别离为,单针接种疫苗28天后为90.07%;单针接种疫苗14天后为95.47%。
科兴中维克尔来福,超700万剂灭活疫苗已供给各省
2021年2月5日,北京科兴中维生物技能有限公司新冠病毒灭活疫苗(商品名:克尔来福®)取得附条件同意上市。该疫苗获批是依据境外Ⅲ期临床试验的成果。科兴中维于二零二零年7月21日起连续挑选在国外的多个国家展开Ⅲ期临床研讨,总入组人数达2.5万人。
在巴西和土耳其两国展开的Ⅲ期临床研讨别离点评了该疫苗在高风险人群(接诊COVID-19患者的医务人员)和一般人群中的维护效能。巴西发布该疫苗维护效能数据显现,到二零二零年十二月16日,疫苗对住院、重症及逝世病例的维护效能为100.00%,对有显着症状且需求医疗干涉的新冠病例的维护效能为83.70%,对包含不需医疗干涉的轻症病例在内的一切新冠病例维护效能为50.65%。土耳其Ⅲ期临床试验成果显现,到二零二零年十二月23日,该疫苗依照0,14天程序接种2剂疫苗14天后防备COVID-19的维护效能为91.25%。
到1月十日,该公司新冠灭活疫苗“克尔来福”已有超700万剂供给到国内各省,并与香港政府签署了100万剂供给协议。
国药中生北京所新冠疫苗,国内首款获批上市疫苗
二零二零年十二月30日,国家药监局附条件同意国药集团我国生物北京生物制品研讨一切限责任公司的新冠病毒灭活疫苗(Vero细胞)注册请求。该疫苗也成为首家获批的国产新冠病毒灭活疫苗。
依据国药集团我国生物北京所发布的新冠病毒灭活疫苗Ⅲ期临床试验期中剖析数据显现,该疫苗接种后安全性杰出,免疫程序两针接种后,疫苗组接种者均发生高滴度抗体,中和抗体阳转率为99.52%,疫苗针对由新冠病毒感染引起的疾病(COVID-19)的维护效能为79.34%。
该新冠疫苗别离于二零二零年十二月9日、十二月13日和2021年2月5日,在阿联酋、巴林、玻利维亚获批注册上市,已在全球范围内34个国家展开接种或紧迫运用。10多个国家元首和政要接种了我国生物新冠疫苗。
此外,我国外交部发言人赵立坚2月25日在例行记者会上泄漏,国际上已有几十个国家认可我国疫苗在当地运用,中方现在现已或正在向53个国家供给疫苗帮助,现已和正向27个国家出口疫苗。与此同时,我国要点人群新冠病毒疫苗接种作业也在顺畅推动,到2月9日24时,全国累计陈述接种4052万剂次。
